在信息时代的不断发展下,人们对癌症的了解不断加深。乳腺癌是全球五大常见癌种之一,位居女性癌症发病率的首位。
近日,据阿斯利康官网报道,Truqap(capivasertib,卡帕塞替尼)联合氟维司群(Faslodex)用于治疗接受内分泌治疗期间或之后出现复发或进展,且存在一个或多个PIK3CA、AKT1或PTEN基因改变的雌激素受体(ER)阳性、HER2阴性的局部晚期或转移性乳腺癌成人患者已获得欧盟(EU)批准,该疗法在2023年11月就已经获得美国食品药品监督管理局(FDA)批准。

截图来源于阿斯利康官网,侵权请联系删除
据了解,此次批准主要是基于CAPItello-291的III期临床数据结果,该试验旨在评估卡帕塞替尼联合氟维司群在雌激素受体(ER)阳性、HER2阴性晚期乳腺癌患者中的疗效与安全性。数据结果已于2023年5月31日发表在《新英格兰医学杂志》内。
在2020年 6 月 2 日至 2021 年 10 月 13 日期间,共有 901例患者入组,其中708名患者接受了随机分组,这708名患者中355名患者接受卡帕塞替尼+氟维司群治疗,353 名患者接受安慰剂-氟维司群治疗。
结果显示:卡帕塞替尼组的中位无进展生存期是安慰剂组的一倍,分别为7.2个月和3.6 个月。

图片来源于“参考资料2”,侵权请联系删除
卡帕塞替尼组和安慰剂组中,存活1.5年的患者比例分别为73.9%和65.0%,两组相差不大。

图片来源于“参考资料2”,侵权请联系删除
该数据表明,Truqap(capivasertib,卡帕塞替尼)联合氟维司群可有效延长患者的无进展生存期。
关于Truqap(capivasertib,卡帕塞替尼)
Truqap(capivasertib,卡帕塞替尼)可抑制所有三种AKT亚型 (AKT1/2/3)。2023年11月,Truqap(capivasertib,卡帕塞替尼)联合氟维司群(Faslodex)获得美国食品药品监督管理局(FDA)批准用于治疗完成辅助治疗一年内或在转移性情况下至少接受一种内分泌治疗后出现进展或复发的激素受体(HR)阳性、人表皮生长因子受体2 (HER2)阴性、伴有一种或多种PIK3CA/AKT1/ pten改变的局部晚期或转移性乳腺癌成年患者。
图片来源于“参考资料3”,侵权请联系删除
乳腺癌“神药”DS-8201(德曲妥珠单抗)显威!超过四成的患者治疗四年后病情仍旧没有进展
HER2 是表皮生长因子受体家族的一部分,可以控制细胞生长。DS-8201(Enhertu,德曲妥珠单抗,T-Dxd)是一种用于治疗晚期癌症的抗体偶联药物(ADC),能够在不伤害自身正常细胞的情况下杀伤肿瘤细胞。2023年获得国家药品监督管理局批准上市,用于治疗HER2阳性的乳腺癌患者。
在DESTINY-Breast03临床研究中,DS-8201有78.9%的患者得到缓解,较对照组翻了一倍。实现部分缓解的患者是对照组的两倍,分别有173例和86例得到部分缓解;而实现完全缓解的患者较对照组更是翻了三倍,有33例患者实现完全缓解,对照组仅有11例。DS-8201组有将近一半的患者治疗三年后病情没有进展,超过四成的患者治疗四年后病情仍旧没有进展。
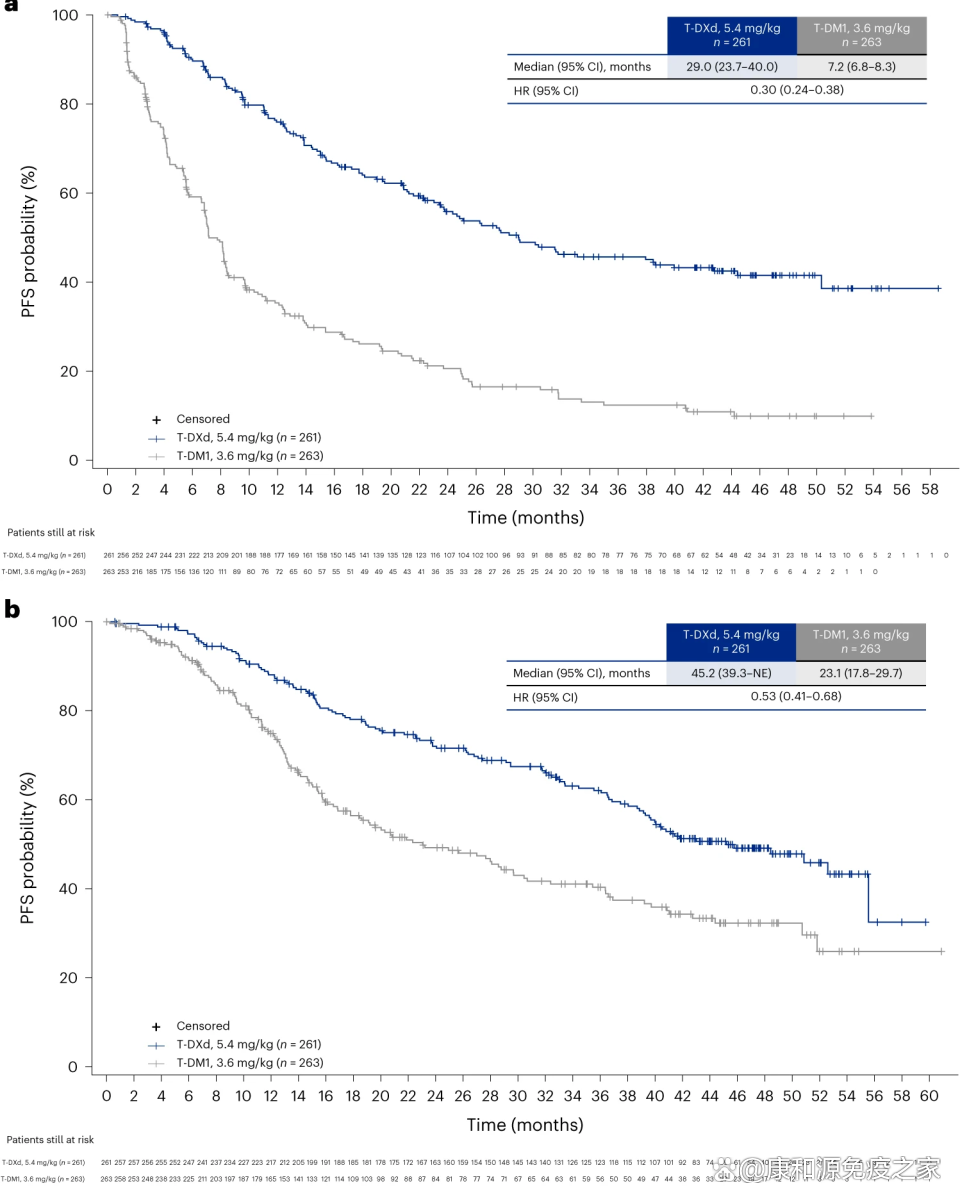
图片来源于“参考资料4”,侵权请联系删除
结语
乳腺癌虽然是女性最常见的癌症,但是科学预防癌症也是会有效降低患癌的风险。在科技水平不断提高的情况下,研究人员针对乳腺癌的治疗方式也在不断的深入,目前乳腺癌死亡率较之前已经有了明显的下降,生活质量也有所改善。期待癌症“治愈”的那一天!
参考资料
1.Truqap plus Faslodex approved in the EU for patients with advanced ER-positive breast cancer (astrazeneca.com)
2.Capivasertib in Hormone Receptor–Positive Advanced Breast Cancer | New England Journal of Medicine (nejm.org)
3.FDA approves capivasertib with fulvestrant for breast cancer | FDA
4.Trastuzumab deruxtecan versus trastuzumab emtansine in HER2-positive metastatic breast cancer: long-term survival analysis of the DESTINY-Breast03 trial | Nature Medicine
免责声明:文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!