“民科”千万别他妈搞化学!

现在很多小视频up主在搬运油管的视频,弄一些做各种化学品的段子。其实油管上的很多国外科普作者和咱们国内的很多情感视频作者一个样,利用各种断章取义的概念和不完全的剪辑、借位、替代手段,硬生生的编造出一大堆不靠谱的概念和消息。
到了咱们这,很多大学光会打游戏、毕业找不到工作的小视频作者就像挖掘到了宝藏一样,剪辑、翻译一下就到咱大中国做“专业科普实验”了?
“民科”千万别他妈搞化学!搞搞物理、数学甚至哲学这些事情在通常的情况下顶多是浪费点时间,搞得大了也就是浪费点公共资源,而化学这玩意如果稍有不慎还真说不好会带走谁。
所以W君就回复了一句——这个不是执着硝化棉的。
后面其实还有句话没打进去——“骗傻子的!”
直接省流——树根清除剂、管道疏通剂再加上脱脂棉就能做出硝化纤维来?这事情是想瞎了心了。
解释下,硝化纤维是利用浓硝酸在浓硫酸的催化作用下脱去纤维素中的羟基利用硝酸的硝酸根进行取代的反应。这里的“浓”并不是大家能尝出咸淡的“浓”而是“极其的浓”。这样说,通常我们在实操的时候是使用98%的浓硫酸配合63%的浓硝酸来做。

这样浓硫酸的脱水作用会带走纤维素中的羟基,同时,浓硝酸中的“硝酸根”会取代纤维素中被剥离掉的羟基位置形成稳定的硝化纤维素。
这个反应的关键点在于浓度,只有在足够浓度的条件下硫酸和硝酸才能呈现出刚刚描述的化学特性。而不是说在溶液中存在硝酸根就能硝化纤维素。
树根清除剂中含有大量的硝酸钾、而管道疏通剂中含有一定量的硫酸。在这个反应过程中理论上是可以生成硝酸的。有这个化学反应方程:
KNO3 + H2SO4 → KHSO4 + HNO3
并不用奇怪的确是有这个方程式,而且理论上硫酸是可以制造出大部分酸的。这个说法并不符合大家初中学到的“强酸制弱酸”的那一条准则。硫酸可以制造更强的酸的前提条件有两个第一是浓硫酸,第二是所制造的目标产物沸点低于硫酸。
浓硫酸很容易满足,我们可以很方便的制备98%的无水硫酸。
目标产物的沸点低于硫酸也很好满足,例如硝酸的沸点只有83摄氏度,而浓硫酸的沸点是337摄氏度,你能想到啥?对喽——蒸馏。蒸馏的过程会使目标产物从反应溶液中迅速分离,分离物中没有硫酸根的介入,因此KNO3 + H2SO4 → KHSO4 + HNO3反应是不可逆的,否则KHSO4 + HNO3 → KNO3 + H2SO4也成立。
再说,纤维素是什么?

如果看中括号以内的部分,就是C6H10O5,大家都熟悉的这就是葡萄糖(C6H12O6)去掉了一个分子的水(H2O)。其实是丢了一个氢离子(H)和一个羟基(OH),于是分子的首尾相连接形成了[C6H10O5]n。这是一种多糖聚合物。

真正的反应式是这样的,注意!硫酸(H2SO4)是放在反应箭头下面的化学方程式中箭头下面是什么?——催化剂。而真正的硝酸根其实并不产参加反应,而是在硫酸的作用下形成(NO₂⁺)这个东西叫做硝酰阳离子,是它取代的羟基,其实这是一个典型的硝酸酯化反应。
这个反应还是会有水产生的,所以反应极限是硫酸的浓度至少在65%以上,硝酸浓度至少在25%以上。树根清除剂和管道疏通剂中根本就不能提供出那么多的硫酸和硝酰。
那么问题来了,为什么最后实验的验证阶段那一撮棉花可以迅速的燃烧呢?

其实烧着的就是树根清除剂里面的硝酸钾。惊不惊喜,意不意外?一顿操作猛如虎、回头一看原地杵。

这是因为在反应中硝酸钾根本没有被消耗和反应,同时,硝酸钾还有一个很有意思的特性就是溶解度随温度变化极大。
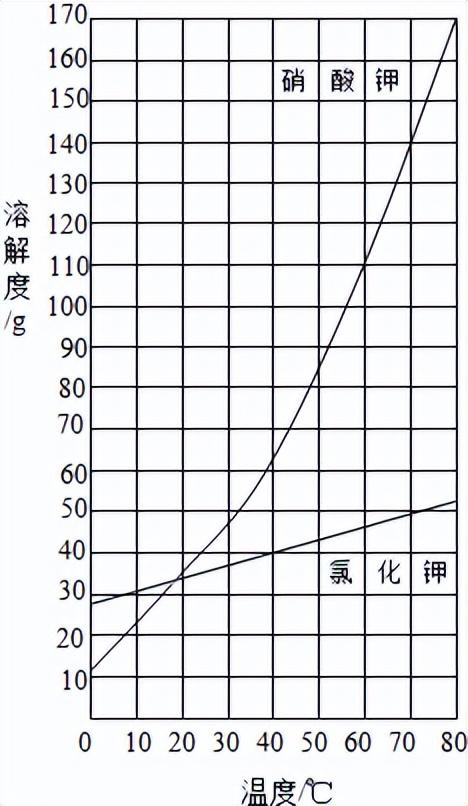
在溶解度曲线上硝酸钾极其陡峭,在后期的水洗过程中又是用的冰水,而且没有洗干净,析出的硝酸钾被棉花的纤维结构所吸收,于是一点起来当然就一大片火苗了。
在真正制造硝化纤维素的过程中产物的清洗工作一般的情况下是先用温水清洗至不呈酸性,在用大量的无水酒精冲洗去除杂醇。
在检验生成物的时候,会用到一定配比的醇醚溶液和丙酮去验证反应生成物。当反应物在两种试剂中均不可溶证明反应失败;如果只溶于丙酮而不能溶于醇醚溶液则证明硝化过度;两种试剂均可溶解反应产物则证明反应成功。
不过也别高兴,这种方法生成的硝化纤维素别说做发射药了,就连做乒乓球都不合格。

基本上这种硝化纤维素就只能拿去做油漆。
这里面就有产物含氮量的问题了,测量硝酸纤维素的含氮量其实也不难,在前面说了,硝化纤维素的硝化过程实际上就是一个典型的硝酸酯化反应。所以硝酸纤维素又叫纤维素硝酸酯。既然是酯就可以发生皂化反应。在这个反应中会释放出氮的氧化物,测量这些氮氧化物的含量就可以推算出这批硝化纤维素的氮含量了。关于怎么促进硝化和测量氮含量就不多写了,这个事情专业之外的人知道的太多不好。
但,按照油管做硝化纤维这件事,咱们还是最好别尝试。不要命之举,不仅仅是有爆炸性危险,还会因为各种不同的家用化学品中的不同配方成分这样无脑的混合搅拌,还不知道会生成什么有毒有害物质,所以这样的操作存粹是玩命。
