AbMole以其卓越的品质、与时俱进的产品、专业无忧的服务,不断鼎力支持全球科学家获得重要的突破性成果。近日由来自华中科技大学同济医学院附属协和医院的Xi Zhang,Heng Xu,Jie Wu和Jiahong Xia等多名研究人员在Circulation期刊(IF=37.8)上,共同发表了题为“Immune Regulation of the Liver Through the PCSK9/CD36 Pathway During Heart Transplant Rejection”的文章。在该文章中,研究人员使用了购自AbMole的Alirocumab(阿利珠单抗,M3835),揭示了心脏移植排斥反应(HTR)期间肝脏通过PCSK9/CD36通路进行免疫调节的新机制,并提示对该通路的调节可能是预防HTR的潜在治疗靶点。

对于心脏移植患者,HTR是患者存活的主要障碍,其特征是促炎巨噬细胞和效应T细胞大量浸润,并伴有心肌细胞损伤。以前的研究通常集中在免疫细胞,但是非免疫器官和相关分子在心脏移植排斥反应中的作用尚未明确。在该文章中通过分析临床患者(如图1A所示),以及完全MHC错配小鼠心脏移植后的血清数据,均发现在HTR期间血清PCSK9水平升高。通过对移植受体小鼠进行多器官筛选和多组学分析,发现在同种异体受体小鼠中,Pcsk9 mRNA在肝脏的表达明显高于其他器官(图1B-D)。
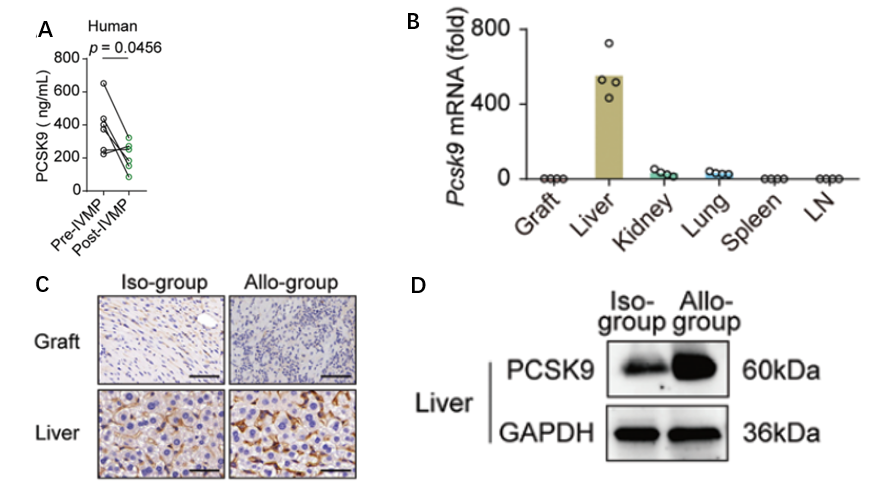
图 1 A ,在静脉注射甲基强的松龙(IVMP)前后,通过ELISA检测心脏移植排斥者的血清PCSK9水平。B,从异体组小鼠的受体器官中提取总RNA并反转录成cDNA。通过qPCR检测Pcsk9相对于Gapdh的mRNA表达水平(n=4)。C,对受体小鼠的移植物和肝脏进行PCSK9的免疫组化染色。比例尺,100μm。D,进行Western印迹检测PCSK9在受体小鼠肝脏中的表达,并使用GAPDH作为内参。之后,对移植后受体小鼠的血清进行了多重细胞因子检测,发现促炎症细胞因子、VCAM-1和M-CSF水平明显增加(图2A)。在体外用这些细胞因子刺激原代小鼠的肝细胞,得出了TNF-α和IFN-γ能诱导PCSK9的mRNA表达(图2B)的结论。

图 2 A , 在心脏移植后第6天,从同源(B6到B6小鼠,同源组)和异源小鼠(BALB/c到B6小鼠,异源组)中收集血清。用ABplex Mouse 18-Plex Custom Panel检测小鼠血清中的多种细胞因子和趋化因子(n=2)。B,从B6小鼠中分离出原代肝细胞,用PBS、TNF-α或IFN-γ培养24小时,并收集Pcsk9 mRNA,用qPCR测定进行分析(n=3)。此外,研究人员还进行了体内研究,通过构建心脏转基因动物模型进行实验,实验结果显示,在HTR期间,Tnf或Ifn缺乏不仅能抑制受体肝脏SREBP2的表达,还可以降低肝脏Pcsk9 mRNA的表达和血清PCSK9水平(图3A和3B),并得到TNF-α和IFN-γ能通过SREBP2协同促进肝细胞中PCSK9的表达(图3C)的结论。

图 3 A和B,在心脏移植后第6天收集受者的肝脏和血清。A, 肝脏中SREBP2的mRNA和蛋白水平通过qPCR(n=4)和WB测量。B, 肝脏中SREBP2的mRNA水平通过qPCR测定,血清中PCSK9的水平通过ELISA测定(n=4)。C,细胞因子(TNF-α和IFN-γ)和信号通路(P65和STAT1)通过转录因子SREBP2调节肝细胞中PCSK9表达。然后,又通过分析包含人心内膜活检数据的微阵列数据集,发现只有CD36的表达在排斥和无排斥移植的心内膜活检中明显不同(图4A,B)。且经单细胞RNA-seq分析,发现CD36主要在移植物浸润巨噬细胞中表达(图4C,D)。

图 4 A-B,分析了人心脏移植活体组织的微阵列数据。A,M-versus-A图显示排斥组和非排斥组的差异表达基因(DEGs,LFC>1,Padjusted<0.05)。PCSK9的靶点,包括LDLR、LRP1、LRP5、LRP8、VLDLR和CD36,被标记出来。B,散点图显示排斥组和非排斥组之间CD36的表达。C-D,在具有完全MHC错配的小鼠中进行心脏移植(BALB/c到B6)。移植后第6天收集异体移植物,并将移植物中的CD45+细胞分类,进行10×基因组学单细胞RNA测序。C,tSNE图描述了心脏浸润的CD45+免疫细胞被分成5组。D,热图显示每个簇中Cd36的表达情况。通过比较用PCSK9处理的腹膜巨噬细胞和对照组,观察到MHCII和共刺激分子表达增加(图5A),以及CD36的表达和脂肪酸的吸收减少(图5B)。结果表明PCSK9不仅能控制CD36表达和脂肪酸摄取,还可以增强巨噬细胞的促炎表型和功能。从而揭示了在HTR期间,肝脏通过PCSK9/CD36通路进行免疫调节的新机制,以及该通路可能是HTR的潜在治疗靶点。

图 5 A, 腹腔巨噬细胞中MHCII、CD80、CD86和CD40的荧光强度值的代表性FACS直方图和条形图(n=4)。B, 腹膜巨噬细胞中CD36表达(左侧,n=5)和BODIPY(右侧,n=5)的代表性FACS直方图和柱状图。在实验中,多次使用购自AbMole的Alirocumab (阿利珠单抗,M3835),Alirocumab是一种全人源的IgG1型PCSK9单抗,通过使用Alirocumab中和B6小鼠的PCSK9,可以延长小鼠的心脏移植存活率,并能减少CD4+、CD8+ T细胞和巨噬细胞的浸润,明显降低移植物中编码免疫细胞、转录因子和与炎症有关的细胞因子的基因水平,并且,Alirocumab在延长异体移植存活率和减弱异体移植排斥反应方面的表现,明显优于他汀类化合物洛伐他汀(图6)。此外,作者还发现用单克隆抗体Alirocumab中和PCSK9会导致小鼠血清PCSK9水平显著升高。从而得出了PCSK9参与心脏移植后的同种免疫反应的结论。

图 6 用Alirocumab(200μg/小鼠,腹腔注射,每2天一次,从心脏移植当天开始)、人IgG1同种型对照或洛伐他汀(100μg/小鼠,每天腹腔注射,从心脏移植当天开始(n=5;log-rank检验)治疗的心脏异体移植的生存曲线。根据2004年ISHLT指南对细胞排斥进行评分(n=6;Kruskal-Wallis检验)。之后,通过使用Cd36–/–小鼠作为心脏移植模型中的受体,并给予Alirocumab处理。如图7A所示,发现在Cd36敲除小鼠中,单克隆抗体治疗对心脏移植物长期存活的能力减弱。由于CD36也在心肌细胞上表达,为了研究上述结果是否与供体心脏中CD36的表达有关,又通过构建HTR小鼠模型,并用同种型IgG1或Alirocumab治疗受体小鼠(图7B)。发现Alirocumab在该模型中显著延长了心脏同种异体移植物的存活时间(图7C)。从而得到PCSK9消融对HTR的保护作用是CD36依赖性的结论。

图 7 A,用Alirocumab治疗的WT和Cd36-/-小鼠异体移植的生存曲线(n=5)。B-C,将WT B6和Cd36-/-小鼠(B6背景)的心脏移植到BALB/c小鼠体内,无论是否经过Alirocumab治疗 B, 动物模型研究的工作流程示意图。C, 经或不经Alirocumab治疗的WT和Cd36-/-小鼠异体移植的生存曲线(n = 5, log-rank检验)。通过多项实验,研究人员发现,在HTR期间,TNF-α和IFN-γ通过转录因子SREBP2协同促进PCSK9在肝细胞中的表达,导致血清中PCSK9水平升高。增加的PCSK9抑制了CD36的表达和巨噬细胞对脂肪酸的吸收,有利于促进供体反应性T细胞的增殖和IFN-γ的产生(图8)。该研究揭示了HTR期间肝脏通过PCSK9/CD36途径进行免疫调节的新机制,并且表明该途径的调节可能是HTR的一个潜在治疗靶点,为PCSK9在同种异体免疫中的作用提供了新的见解。

图 8 在HTR过程中,肝细胞和移植物浸润巨噬细胞之间通过PCSK9/CD36途径相互作用的模型。AbMole产品涵盖抑制剂/激动剂、细胞因子、人源化单抗、活性肽、天然产物、化合物库等各种热门类别,数万个产品现货储备,发货快捷,服务专业。鸣谢:Zhang, Xi et al. “Immune Regulation of the Liver Through the PCSK9/CD36 Pathway During Heart Transplant Rejection.” Circulation, 10.1161/CIRCULATIONAHA.123.062788. 26 May. 2023, doi:10.1161/CIRCULATIONAHA.123.062788
