多年来,手术、化疗、放疗以及靶向药物等是癌症治疗的常用方法,抗体偶联药物(ADC)是一种很有前途的癌症治疗新型疗法,通过将细胞毒性有效载荷靶向肿瘤细胞。在单克隆抗体与靶抗原结合时,ADC被内化到肿瘤细胞中。最终的接头分解会促进有效载荷的细胞内释放,并在细胞内发挥其破坏微管或DNA的作用,是目前肿瘤领域发展最快的药物之一。
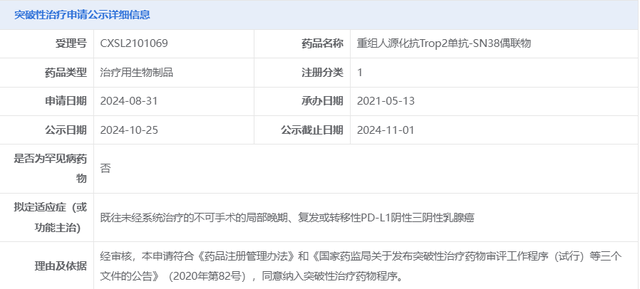
1.乳腺癌-ESG401ESG401是重组人源化抗Trop2单抗-SN38偶联物,在治疗局部晚期或转移性实体瘤患者的1a期临床(NCT04892342)中,ESG401显示出有前景的抗肿瘤活性。该数据结果发表于《Cell》。该试验共纳入40例患者,其中转移性激素受体阳性(HR+)人表皮生长因子受体 2(HER2)阴性乳腺癌(HR+/HER2−BC)患者和三阴性乳腺癌(TNBC)患者均18例,HER2+乳腺癌2例,子宫内膜癌(EC)和腺样囊性癌(ACC)各1例,结果显示:34.2%的患者肿瘤缩小或消失,临床获益率(CBR)为 50.0%,25例患者病情得到控制,疾病控制率(DCR)为 65.8%,中位缓解持续时间(DOR)为 6.3 个月,中位无进展生存期(PFS)为 5.1 个月。

截图源于参考资料2
该药物于近日被国家药品监督管理局药品审评中心纳入突破性治疗品种,用于既往未经系统治疗的不可手术的局部晚期、复发或转移性PD-L1阴性三阴性乳腺癌。
SHR-A2009是一款HER3 ADC药物,2024年欧洲肿瘤内科学会(ESMO)年会上公布了SHR-A2009治疗EGFR突变的非小细胞肺癌(NSCLC)患者的I期研究数据。该试验共126例患者接受治疗,结果显示:48例患者肿瘤缩小,62例患者病情稳定(SD),88.9%的患者病情得到控制,中位缓解持续时间(DOR)为8.2个月,中位无进展生存期(PFS)为6.9个月。


截图源于参考资料3
接受7.5mg/kg剂量组治疗的12例患者中,4例患者肿瘤缩小,7例患者病情稳定(SD),疾病控制率(DCR)高达91.7%,中位缓解持续时间(DOR)为12.3个月。
接受9.0mg/kg剂量组治疗的49例患者中,23例患者肿瘤缩小,23例患者病情稳定(SD),疾病控制率(DCR)高达93.9%,中位缓解持续时间(DOR)为8.3个月。
接受7.5-9.0mg/kg治疗的94例患者中,38例患者肿瘤缩小,50例患者病情稳定(SD),疾病控制率(DCR)为93.6%,中位缓解持续时间(DOR)为8.3个月,中位无进展生存期(PFS)为9.6个月。
3.铂耐药卵巢癌(PROC)-SHR-A1921SHR-A1921是一款以TROP-2为靶点的抗体药物偶联物(ADC),SHR-A1921治疗铂耐药卵巢癌(PROC)的首次人体I期研究中,接受3.0mg/kg剂量组治疗的26例患者均实现疾病控制,疾病控制率(DCR)高达100%,42.3%的患者得到客观缓解,中位缓解持续时间(mDoR)为9.9个月,中位无进展生存期(mPFS)为7.9个月。接受2.0+2.0mg/kg剂量组治疗的20例患者中有58.8%的患者实现客观缓解,疾病控制率(DCR)为94.1%,中位缓解持续时间(mDoR)为6.3个月,中位无进展生存期(mPFS)为6.9个月。


ZL-1310是一款靶向Delta样配体3(DLL3)的新一代抗体偶联药物(ADC),在ZL-131治疗广泛期小细胞肺癌(ES-SCLC)患者中的全球1a期临床研究中,19例广泛期小细胞肺癌(ES-SCLC)患者有74%的患者实现客观缓解,14例患者均为部分缓解(PR),3例患者病情稳定(SD)。

截图源于参考资料4
5.尿路上皮癌-维迪西妥单抗维迪西妥单抗是我国自主研发的一款抗体偶联药物(ADC),在维迪西妥单抗联合帕博利珠单抗在未经治疗的HER2有表达的局部晚期或转移性尿路上皮癌的RC48-G001研究中,20例患者有7例实现完全缓解(CR),8例患者实现部分缓解(PR),4例患者病情稳定(SD),75%的患者肿瘤缩小或消失。

截图源于参考资料5
6.胃癌-德曲妥珠单抗优赫得(德曲妥珠单抗,DS-8201,Enhertu,T-Dxd)是一款靶向HER2的新型ADC药物,是ADC药物的杰出代表。II期DESTINY-Gastric01试验中,51%的患者肿瘤缩小或消失,86%的患者病情得到控制,中位缓解持续时间(DOR)为11.3个月。

截图源于参考资料6
该药物已在国内获批用于HER2阳性胃癌患者以及乳腺癌和肺癌患者。
结语
ADC药物是癌症治疗的热点领域之一,目前国内外均在积极探索探究中,相信随着技术的不断精进,ADC药物将更进一步的造福癌症患者,改善患者的生活质量,延长患者生存期,让越来越多的患者有药可吃。
参考资料
1.https://ascopubs.org/doi/10.1200/EDBK_390094
2.https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00428-2
3.https://www.bing.com/ck/a?!&&p=4cc0bcd1134e3c68a0a7dc17f19738244f2bafdf2048245369bcaa02a9a4e15cJmltdHM9MTczMDY3ODQwMA&ptn=3&ver=2&hsh=4&fclid=16e7598d-50d6-6a3a-21d7-4dbe519c6b9d&psq=Phase+I+study+of+SHR-A2009%2c+a+HER3-targeted+ADC%2c+in+pretreated+EGFR-mutated+NSCLC&u=a1aHR0cHM6Ly9jc2xpZGUuY3RpbWVldGluZ3RlY2guY29tL2VzbW8yMDI0L3B1YmxpYy9kb3dubG9hZF91cGxvYWRlZF9tZWRpYS9wZGYvNDY0Nw&ntb=1
4.https://ir.zailaboratory.com/static-files/a26d65b9-34a3-4778-b88f-60c5f5344ee9
5.https://www.urotoday.com/conference-highlights/esmo-2024/esmo-2024-bladder-cancer/154846-esmo-2024-preliminary-efficacy-and-safety-of-disitamab-vedotin-dv-with-pembrolizumab-p-in-treatment-tx-naive-her2-expressing-locally-advanced-or-metastatic-urothelial-carcinoma-la-muc-rc48g001-cohort-c.html
6.https://www.nejm.org/doi/10.1056/NEJMoa2004413?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
免责声明:文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!
