仅供医学专业人士阅读参考
点击右上方“关注”,准时接收每日精彩内容推送。
全球范围内,关节软骨(AC)缺陷是一个常见问题,它们可能在疾病的后期导致关节崩溃,因此需要立即干预以防止软骨的进一步退化。数十年来对水凝胶在生物医学应用的研究揭示了其巨大潜力,特别是在软组织工程领域,包括关节软骨再生(CR)。水凝胶具有高度可调性,可以设计满足CR模板所需的关键标准。
来自德国罗斯托克大学的 Hermann Seitz等团队综述了水凝胶设计在CR领域的前沿进展。本文旨在确定这些标准,包括水凝胶成分、机械性能、生物降解性、结构设计和与邻近原生组织的整合能力,并深入探讨通过适当设计CR可以获得的好处。文章还讨论了模拟天然软骨结构的分层结构水凝胶以及环境刺激对再生结果的影响。通过审视最新进展和新兴技术,本文为开发有效的基于水凝胶的AC修复疗法提供了宝贵的见解。相关工作以题为“Advancements in hydrogel design for articular cartilage regeneration: A comprehensive review”的综述文章发表在2024年09月14日的期刊《Bioactive Materials》。

1.创新型研究内容
根据交联化学的不同,制造出的水凝胶既可以是可植入的也可以是可注射的(见图1)。可植入的水凝胶支架具有显著的临床优势,包括高机械强度和可定制的形状。这些支架通过如3D打印技术(挤出或直接墨写(DIW)方法)预制,并在目标部位进行外科植入,展示了在治疗应用中的巨大潜力。由于其溶胶-凝胶特性,可注射的水凝胶可以轻松填充软骨缺陷。这些对温度或剪切力响应的水凝胶确保了不规则膝关节形状的适当填充、细胞的均匀分布,并使得可以进行微创手术。水凝胶的优势在于其可调性,其属性可以根据应用需求进行调整。
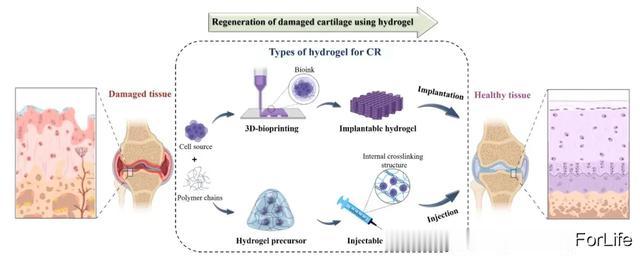
图1 使用水凝胶进行软骨组织再生的方法示意图以及设计用于放置在膝关节损伤部位的不同水凝胶
关键参数,包括材料类型、机械强度、基质刚度和弹性、生物降解性、完整性、孔隙率以及互连性,对于调控细胞命运至关重要,特别是在增殖和分化方面。这为研究开辟了广阔的领域,以确定这些因素单独或相互结合如何有助于更好地重建组织。然而,关于这一领域的基本处理参数的研究却很少。当前的综述文章为水凝胶在这一领域的研究提供了不同的视角。本综述的主要目的是展示设计用于软骨再生(CR)的水凝胶所涉及的关键因素的最新进展。以下部分涵盖了水凝胶设计的参数,包括水凝胶成分、机械性能、生物降解性、结构设计和与相邻天然组织的整合能力。本文首先全面概述了该领域的现有知识,强调了基于水凝胶的软骨组织工程方法的挑战和局限性。然后探讨了水凝胶设计的最新进展和突破,第3节探讨了模仿天然软骨结构的分层结构水凝胶。接下来是讨论环境刺激以及如何通过阐明水凝胶结构之间的相互作用来设计它们以调节细胞反应和组织再生。图2提供了整个综述内容的全面总结。本文旨在强调仿生水凝胶可以恢复关节软骨的组成、结构和生物力学功能。最后通过分享对水凝胶设计用于关节软骨修复未来的看法来结束本文。这些进步在满足尚未解决的临床需求、提高软骨相关疾病患者的生活质量方面具有重大前景,从而直接影响联合国可持续发展目标。

图2 用于软骨再生的水凝胶设计中的关键参数示意图,包括水凝胶成分、机械性能、生物降解性、孔隙性和连通性以及与邻近原生组织的整合
【水凝胶成分】
为了确保实际应用中的生物活性和生物相容性,用于水凝胶的聚合物可以来源于生物体内的内源性物质。这些包括糖胺聚糖、大分子蛋白质和DNA核苷酸。Zhao等人介绍了具有可调节表面硬度的DNA-SF DN水凝胶。这些水凝胶通过DNA碱基配对形成,并通过限制和聚集SF分子促进β-折叠结构的形成。第二网络是通过酶介导的SF交联建立的。研究发现,DNA-SF DN水凝胶在促进软骨分化方面非常有效。在此基础上,Shen等人开发了能够装载BMSCs的RGD-SF-DNA水凝胶微球(RSD-MSs)。首先,使用微流控技术、丝素甲基丙烯酸酯和超分子DNA水凝胶技术创建了SF-DNA DN水凝胶微球(SD-MSs)。然后通过光聚合技术对这些微球进行表面修饰,引入Pep-RGDfKA。结果表明,RSD-MSs是制造和维护长期软骨类器官的理想选择,为CR提供了一个创新的策略和生物材料选择(图3A)。
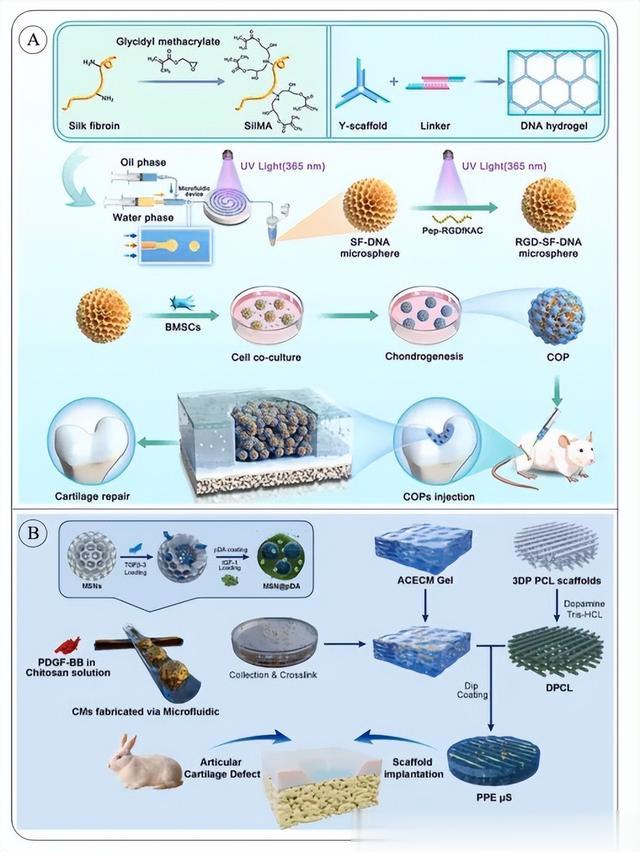
图3 用于合成RGD-SF-DNA微球及其在创建软骨类器官前体和软骨再生中的应用的示意图
【机械强度】
天然的关节软骨(AC)具有独特的机械性能,包括特定的压缩强度、弹性模量和粘弹性行为。水凝胶支架的机械特性在提供适当的支持、负荷分布和功能性方面起着至关重要的作用,这些都是成功进行CR所必需的。许多研究专注于调节水凝胶的机械性能以模拟天然软骨的特性。与常规水凝胶不同,关节软骨既坚硬又坚韧,而常规水凝胶在机械力的作用下会变形,且缺乏软骨修复所需的必要属性。更常见的是,通过牺牲吸收和保留凝胶水分的能力来实现硬化过程,这可能会通过阻碍细胞迁移和生物分子扩散来损害嵌入细胞的存活能力。此外,它们的脆性抑制了力分布,降低了润滑功能。然而,孔径大小、溶胀比、强度和韧性等参数可以在不牺牲硬度的情况下得到改善。Gan等人通过将多巴胺甲基丙烯酸酯低聚物掺入GelMA中开发了一种水凝胶,与单网络GelMA水凝胶相比,该水凝胶在机械性能上具有两个关键优势。首先,GelMA链之间距离的增加提高了水凝胶的失效应变。其次,多巴胺创建了一个次级交联网络,在负载下通过物理牺牲键耗散能量(见图4A)。当前的努力集中在开发既能保持硬度又能分散能量以防止在受损区域集中力量的坚韧水凝胶上。一种有前景的软骨修复方法涉及使用多种聚合物和交联机制,每种都有其特定用途。

图4 多巴胺甲基丙烯酸酯及其低聚物(ODMA)的合成
【刚度和弹性】
基质弹性可以决定干细胞的命运或谱系承诺。在较硬的基质上,MSCs、成纤维细胞和内皮细胞都表现出了改善的细胞粘附、扩散和增殖。如前所述,天然凝胶由于其调整机械性能的能力有限,并不理想用于研究软骨细胞对需要精确控制刚度的基质的力学感应。通过改变交联类型、复合材料的浓度比例、外部刺激、分子量以及添加纳米颗粒(NPs),研究人员创建了可调刚度的水凝胶。Kwon和Yasuda开发了磺酸盐涂层的聚丙烯酰胺(S-PAAm)凝胶,其弹性模量分别为1, 15和150 kPa。培养在高刚度凝胶上的MSCs显示出强烈的应力纤维表达,而那些在低刚度凝胶上的细胞则呈现出圆形,具有更多的皮质肌动蛋白。值得注意的是,较低刚度的凝胶即使没有分化补充剂也导致了更高的软骨生成标记物(Col 2a1, Agc, Sox9)的mRNA水平(图5A)。Lin等人通过调整PEG-二丙烯酸酯(PEGDA)前体的分子量从3.4到20 kDa,创建了具有不同机械性能的水凝胶。较高分子量的PEGDA增加了水凝胶的溶胀比和网格大小。PEGDA-6 kDa和-10 kDa水凝胶在第四周时具有最高的糖胺聚糖(GAG)含量,而PEGDA-20 kDa则有更高的胶原蛋白含量。PEGDA-10 kDa显示出最高的II型胶原过度表达。Schuh等人使用经过RGD修饰的琼脂糖水凝胶独立研究了基质刚度、粘附位点密度和孔隙率的影响。无论基质的刚度如何或粘附位点的可用性如何,细胞都保留了软骨生成表型。通过定量测定发现,经RGD和RGE(精氨酰-甘氨酰-谷氨酰)修饰的较软凝胶中的GAG和DNA含量显著更高。然而,每个DNA的GAG含量不受基质刚度或粘附位点可用性的影响。根据苏木精和伊红(H&E)染色,较软凝胶中细胞ECM簇的平均直径显著大于较硬凝胶中的直径(图5B)。

图5 不同刚度S-PAAm凝胶上MSCs中的F-actin结构以及MSCs在PS(对照)和S-PAAm凝胶上1周后的Col 2a1、Agc、Sox9和Sca1基因表达
【孔隙性与连通性】
优化水凝胶支架的孔隙性和连通性可以通过多种方法实现。一种方法是牺牲模板法,即将某种材料引入水凝胶中,随后去除该材料以形成孔隙。例如,Konka等人在羟基磷灰石支架中使用了Gel微球,从而形成了适合组织工程的多孔结构(图6A)。另一种方法是颗粒沥滤法,即在水凝胶中分散水溶性颗粒,然后溶解这些颗粒以形成孔隙。此外,还使用PLGA海绵作为模板来创建具有连通孔隙的Col支架。这些支架支持均匀的软骨细胞分布、快速的细胞分裂以及增加的软骨基因表达和细胞外基质分泌。最有效的结果是使用高重量比和大盐颗粒的PLGA海绵作为模板的Col支架(图6B)。

图6 使用DIW技术开发分层多孔仿生羟基磷灰石支架
为了创建大孔结构,已经开发了各种其他方法,包括3D打印、冻干法、气体发泡、聚合物相分离以及乳化液滴或聚合物微球。在众多3D生物打印策略中,挤出式打印、喷墨式打印和激光生物打印是最常用的(图7)。每种方法都有其优缺点,例如成本、精度和时间效率。这些标准3D生物打印技术的主要区别在于它们对微观几何结构的精确控制能力。在打印之前,CAD软件系统设计3D模型并设置参数。不同的墨水和方法需要特定的参数。水凝胶墨水被混合并放置在墨水储存盒中,然后由3D打印机逐层应用到构建平台上。每一层硬化后,再添加下一层,逐步构建起3D水凝胶前体,最后将其连接在一起。然而,在空中打印软质生物材料可能导致变形和形状丧失。为解决这一问题,自由可逆嵌入悬浮水凝胶(FRESH)技术在具有屈服应力的支持浴中打印生物墨水,该支持浴在生物墨水固化前将其固定住。该方法涉及将打印的水凝胶嵌入作为临时性、热可逆性和生物相容性的第二水凝胶中。

图7 生物打印步骤和不同打印方法的示意图
组织发育的不同阶段需要不同的大孔密度和大小。低孔隙度提供结构稳定性并保存移植细胞,而随着时间的推移增加的孔隙度有助于营养扩散、细胞增殖和基质形成。张等人开发了一种具有膨胀依赖性门控的双层3D打印支架,其下层孔隙较小,上层基质孔隙较大。这种设计允许骨髓MSCs最初浸润,随后阻断过多的血液支持,有助于稳定的软骨生成(图8A)。可生物降解聚合物可以随时间增加孔隙度,但控制大孔形成的时机和程度仍然具有挑战性。现有方法通常使细胞暴露在恶劣条件下,降低存活率。在预制的大孔支架上接种细胞可能导致效率低下和分布不均。使用非细胞毒性成孔剂封装细胞可以更好地控制细胞分布。韩等人使用刺激响应性成孔剂创建了具有可调大孔的动态水凝胶,响应温度、螯合和酶解等刺激。

图8 用于软骨修复的具有两种孔径的双层支架示意图
【整合能力】
可注射水凝胶以其易于给药和对刺激的响应性而闻名,通过均匀分散细胞和生物分子并填充不规则的组织缺陷,促进与周围软骨的整合。调整凝胶时间对于强整合至关重要;它既不应过长以避免材料流动,也不应过短以免影响整合。可注射水凝胶也用于治疗复杂的疾病如骨关节炎,其剪切稀化特性防止细胞沉降。Hou等人将脲嘧啶酮(UPy)单元掺入DEX聚合物中,创建了一种剪切稀化的水凝胶,由于动态氢键作用,在几分钟内就能整合两种嵌入软骨细胞和BMSCs的水凝胶(见图9A)。

图9 用于多组织复合再生的DEX-UPy水凝胶设计
【总结与展望】
水凝胶的机械性能,如刚度和弹性,必须与天然软骨紧密匹配,以有效分配负载并与周围组织整合。平衡刚度、韧性和弹性是具有挑战性的,因为改善其中一个往往会牺牲另一个。例如,增加刚度可能会减少水分保持能力,而这对细胞存活至关重要。需要创新的方法,如多网络水凝胶或动态共价键,来创建能够承受关节复杂机械环境的同时支持组织再生的水凝胶。此外,这些材料必须与细胞封装兼容且无毒。生物降解性也是关键;水凝胶必须以允许结构支持的速率降解,同时逐渐被新的ECM替代。孔隙率和互连性对于细胞浸润、营养扩散和废物清除至关重要,这些都是功能性组织形成所必需的。先进的水凝胶采用策略如酶促降解片段和微腔结构来增强基质分布和软骨细胞增殖。然而,与宿主组织的整合仍是一个主要挑战,特别是由于软骨的密集ECM和关节的苛刻机械环境。研究集中在通过生物粘合剂、用吸引细胞成分修改水凝胶以及优化孔结构以支持细胞迁移和ECM沉积来改善整合。克服这些挑战对于释放水凝胶在软骨修复中的全部潜力并确保其成功临床应用至关重要。
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯
