胆管癌是一种恶性肿瘤,起源于胆道系统的上皮组织。这种疾病常常被称为“寂静的杀手”,因为它的早期症状不明显,临床表现模糊,导致该疾病在早期难以诊断。然而,随着医学科技的发展,越来越多的治疗方法出现在胆管癌患者的治疗方案中,其中包括了一些令人充满期待的新疗法,如抗体偶联药物(ADC)、光动力疗法(PDT)和光免疫疗法(PIT)。
一、
抗体偶联药物(ADC):精准打击胆管癌
抗体偶联药物(ADC)是一种新型的肿瘤治疗方法,它将单克隆抗体、细胞毒素和连接剂巧妙地结合在一起。这种复合物能够精准地识别并攻击胆管癌细胞,同时对正常细胞几乎没有副作用。三个试验分别研究了针对HER2、MUC1和GPC1的ADC用于CCA治疗。

1
针对HER2的ADC治疗
一项针对HER2的ADC治疗试验,采用HER2阳性的CCA细胞作为靶点。研究结果显示:ADC药物trastuzumab emtansine(T-DM1)对表达HER2水平较高的CCA细胞具有较强的抗增殖作用。此外,T-DM1还显示出了在HER2阳性非小细胞肺癌、唾液腺癌、子宫内膜癌和胆道癌中的治疗潜力。其中,有两例患者的肿瘤缩小程度达到了60%以上。鉴于这一结果,目前日本正在进行HER2阳性不可切除或复发性胆道癌的多中心II期试验,以评估T-DM1的治疗效果。
2
针对MUC1的ADC治疗
MUC1是一种广泛表达在腺癌中的上皮粘蛋白抗原,包括胰腺癌、胃癌、卵巢癌和胆道癌。一项针对MUC1的ADC治疗试验,将staphylococcal enterotoxin A(SEA)与针对MUC1的抗体(MUSE11)结合,以靶向CCA细胞。结果显示:该ADC药物能够增强淋巴细胞活化杀伤细胞(包括NK、NKT和T细胞)对CCA的作用。因此,SEA-MUSE11药物偶联物可以通过上述机制独立对CCA细胞产生抗癌活性。
3
针对GPC1的ADC治疗
GPC1是与细胞表面连接的一种肝素硫酸蛋白聚糖,通过作为共受体促进肿瘤生长、转移和侵袭GPC1肝外胆管癌中高度表达。一项针对GPC1的ADC治疗临床前研究显示:MMAF-结合的抗GPC1抗体能够在体外和体内强效抑制GPC1阳性的CCA细胞的肿瘤生长。注:MMAF是一种微管聚合抑制剂,也被广泛用于治疗复发或难治性多发性骨髓瘤。

二、
光动力疗法(PDT):用光线消灭癌细胞
自古埃及时代以来,光线在医学领域就被用于治疗皮肤疾病,如白癜风和银屑病。如今,光动力疗法(PDT)广泛应用于传染病学、皮肤科学、妇科学、泌尿学和肿瘤学等领域。

PDT的现代医学概念最早是在1900年由Raab和von Tappeiner提出的,当时他们偶然发现PDT可以治疗疟疾引起的原虫。据文献记载,PDT在人类肿瘤治疗方面的第一个应用是在1903年由von Tappeiner为皮肤肿瘤进行的。近70年后,Diamond等人发表了一篇开创性的报告,证明了PDT对大鼠胶质瘤的抗癌作用,在体内和体外的实验都取得了显著的成果。PDT的作用范围局限于光敏剂和白光共存的区域,从而实现高度靶向治疗。
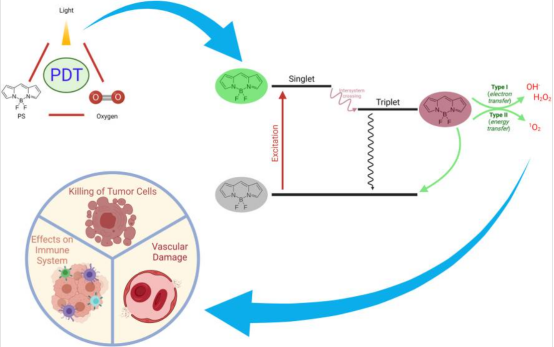
PDT的工作机制包括以下几个阶段:(1)光敏剂进入细胞;(2)光敏剂从基态激发到激发态;(3)光敏剂向周围生物分子(I型反应)或氧分子(II型反应)转移能量;(4)产生活性氧(ROS):I型反应产生超氧阴离子自由基(O2•−)和羟基自由基(OH•),II型反应产生单线态氧(1O2);(5)氧化应激导致癌细胞的破坏。近期的研究还发现,PDT可能通过凋亡和坏死引发免疫原性细胞死亡,释放出损伤相关的分子,激活适应性免疫应答。
PDT在1976年进行了首次人体试验,研究人员使用了血卟啉衍生物(HpD)治疗了5例膀胱癌患者。目前,PDT已被批准用于治疗多种癌症,包括头颈部、脑、肺、食管、乳腺、前列腺、膀胱、皮肤、胰腺和胆管癌等。1975年,Dougherty等人进行的关键研究表明,HpD在体内展示了PDT的高抗肿瘤效果,而单独的HpD或单独的光线则没有效果。之后,各种光敏剂相继问世。第二代光敏剂(血卟啉衍生物和合成光敏剂)开发出来以解决第一代光敏剂的缺陷,如化学纯度低和在相对短波长(630nm)处最大吸收导致的组织穿透性差。第三代光敏剂包括与抗原特异性靶向的分子和脂蛋白相结合的第二代光敏剂,这些方法增加了癌细胞的亲和力和渗透性,降低了对皮肤的毒性。目前,HpD、丙卟啉、叶绿酸、锌血卟啉和含氯类光敏剂被广泛用于临床和临床前的胆管癌治疗研究。

光源方面,PDT的光源也在不断发展。最初,采用非激光光源,如传统灯具。然而,这些光源存在一些局限性,例如难以准确计算输送的光剂量。近年来,激光器的发展使得PDT的光源更加高效,激光器可以产生已知波长的单色光,并且可以通过光纤进行局部治疗。此外,半导体二极管技术的进步使得激光系统变得更加廉价。因此,目前激光器和光发射二极管(LEDs)成为了PDT的首选光源。
三、
光免疫疗法(PIT):瞄准癌细胞的新希望
光免疫疗法(PIT)是一种新型的抗癌疗法,是由日本科学家小林浩等人于2011年开发的。理论上,PIT可以选择性地杀死靶向的癌细胞,对正常细胞没有损害。
PIT包含一种特殊的光敏剂称为“IR700”。这种水溶性光敏染料由硅酞菁和亲水性侧链(IRDye 700DX N-羟基琥珀酰亚胺酯)组成。此外,PIT还结合了一种特定的分子,使其能够与目标细细胞结合,这种分子可以是抗体或低分子量化合物。例如:IR700可以与抗表皮生长因子受体(EGFR)抗体或与IR700结合的affibody-光敏染料共轭物(APCs)相结合。IR700与常规光敏剂相比,具有更高的消光系数,使其在近红外光谱(NIR)范围内具有更高的吸收能力,从而增强了PIT的效果。

PIT的作用机制与PDT有所不同。在PIT中,IR700-APCs与细胞结合后,经过近红外激光照射后,IR700发生化学变化,释放出亲水性侧链。这些物质的聚集导致形成不溶于水的APCs或APC-抗原复合物,并损伤细胞表面的分子,特别是跨膜靶标蛋白。接着,水流进入细胞质,导致细胞肿胀并最终死亡。相比之下,PDT的作用机制是通过产生活性氧来破坏细胞内部结构。
PIT不仅可以直接杀死癌细胞,还能诱导免疫原性细胞死亡,通过释放肿瘤抗原来刺激免疫细胞,增强宿主的抗癌免疫应答。因此,PIT不仅对目标细胞具有杀伤作用,还可以促进宿主免疫系统对肿瘤的攻击。
目前,PIT已经在头颈部癌症治疗方面取得了一定的成功。在日本,PIT已经被批准用于治疗局部晚期和复发性头颈部癌,并在美国进行了针对相同癌症的III期临床试验。此外,PIT也在胃癌、食管癌和实体瘤治疗方面展现了潜力。然而,目前尚未有PIT在胆管癌患者中进行的临床试验。
虽然PIT为治疗胆管癌提供了新的希望,但目前仍面临一些挑战。其中之一是如何将PIT的光敏剂有效地递送到深层的肿瘤组织中,尤其是对于难以接触和可视化的外肝和内肝胆管癌。针对这个问题,一种专用的PIT装置可能是解决方案之一,例如可以通过特殊导管(如胆道引流管)在外围胆管癌处进行PIT治疗。
综合而言,ADC、PDT和PIT是近年来兴起的胆管癌治疗方法,它们通过不同的机制针对癌细胞,具有精准、高效、低毒副作用等优点。然而,这些新疗法目前还处于研究阶段,需要进一步的实验和临床试验验证其安全性和疗效。随着科学技术的不断进步,相信这些新疗法将为胆管癌患者带来更多的希望,为这个艰难的战斗增添新的武器,让患者迎来更美好的未来。
来源:国际肝胆资讯